Постановлением правительства РФ от 23 февраля 2018 года №189 утверждены правила предоставления субсидии из федерального бюджета федеральному государственному автономному учреждению «Российский фонд технологического развития» на реализацию проектов по внедрению системы мониторинга движения лекарственных препаратов.
Документ подготовлен Минпромторгом России в соответствии с приоритетным проектом «Внедрение автоматизированной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя для защиты населения от фальсифицированных лекарственных препаратов и оперативного выведения из оборота контрафактных и недоброкачественных препаратов».
Как писал D-Russia.ru, федеральным законом от 28 декабря 2017 года №425-ФЗ внесены изменения в федеральный закон «Об обращении лекарственных средств», которыми предусматривается создание системы мониторинга движения лекарственных препаратов для медицинского применения. Положение об обязанности производителей наносить средства идентификации на упаковку лекарственных препаратов для медицинского применения вступает в силу с 1 января 2020 года.
Как следует из постановления №189, средства фонду будут предоставляться в рамках государственной программы «Развитие фармацевтической и медицинской промышленности» на 2013–2020 годы.
Субсидия будет предоставляться на основании соглашения Минпромторга России с фондом в соответствии с типовой формой, которая утверждается Минфином России.
Фонд за счёт субсидии будет предоставлять целевые займы российским юридическим лицам на реализацию таких проектов. Договор на эту работу должен предусматривать в том числе использование займа на перевооружение производства лекарственных препаратов, включая приобретение оборудования и программного обеспечения, опытно-конструкторские работы, инженерные изыскания.
Порядок отбора проектов и проведения экспертизы заявок на получение займов будет определяться фондом по согласованию с Минпромторгом России.
Паспорт приоритетного проекта «Лекарства. Качество и безопасность» (полное название - «Внедрение автоматизированной системы мониторинга движения лекарственных препаратов от производителя до конечного потребителя для защиты населения от фальсифицированных лекарственных препаратов и оперативного выведения из оборота контрафактных и недоброкачественных препаратов») утверждён по итогам заседания президиума Совета при президенте России по стратегическому развитию и приоритетным проектам 25 октября 2016 года.
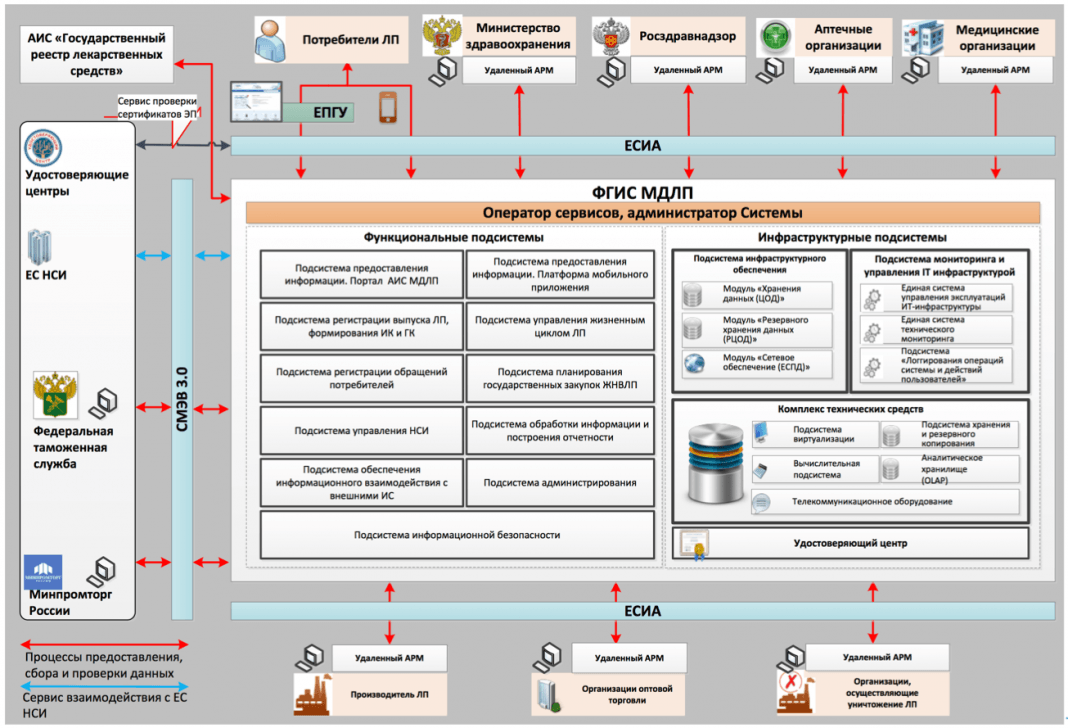
Проект рассчитан на срок с 25 октября 2016 года по 1 марта 2019 и разбит на два этапа. На первом (с 1 января 2017 года до 31 декабря 2017) было запланировано провести на территории РФ эксперимент по маркировке контрольными знаками (RFID-метками) лекарственных препаратов для медицинского применения на добровольной основе для ограниченного набора препаратов преимущественно из перечня 7ВЗН («Семь высокозатратных нозологий») на полной модели товарной цепи от производителя до конечного потребителя. По данным ФНС, на декабрь 2017 в системе маркировки лекарств было зарегистрировано 430 крупнейших представителей фармотрасли и промаркировано более 2,6 миллиона упаковок лекарственных препаратов. Также ФНС запустила бесплатное мобильное приложение «Проверка маркировки товаров», с помощью которого можно узнать о легальности маркированного товара.
На втором этапе (с 1 января 2018 года до 31 декабря 2018) должна быть введена обязательная маркировка всех 100% лекарственных препаратов. Однако согласно №425-ФЗ, срок маркировки 100% лекарственных средств и полномасштабное использование системы (срок завершения второго этапа) перенесен на 1 января 2020 года, таким образом внедрение системы продлено на один год.

















